美国FCN认证返回 Back
美国FCN认证
市场准入通知程序(Premarket Food Contact-substance Notification, FCN):如果一种食品接触性物质对食品没有渗移或极少渗移,则可采用FCN程序申请FDA许可,提交相关化学及毒理学信息以证明其使用的安全性。

美国食品和药品管理局(FDA)在修订1997年《食品和药品监督管理局现代化法案》(FDAMA)中关于食品接触物质(FCS)上市前通知程序的食品添加剂法规。通知程序是批准FCS食品添加剂新用途的主要方法。食品和药物管理局正在编纂法规,以确定在何种情况下需要食品添加剂申请(FAP)来批准FCS的使用;指定FCS通知中所需的信息;描述通知流程的管理;并制定机构认为通知不再有效的程序。
美国食品和药物管理局(FDA)的职责之一是监管食品接触材料的成分,包括包装。曾经被称为间接食品添加剂的FDA现在将这些材料称为食品接触物质(FCS)。为了确保这些物质的安全使用,FDA在食品安全和应用营养中心(CFSAN)食品添加剂安全办公室内建立了食品接触通知计划。本文描述了如何向FDA提交FCS通知,以及食品接触通知审查流程是如何工作的。它还讨论了参与事先通知磋商的重要性、法规豁免门槛的作用以及保密问题。

定义、历史和范围
定义。《联邦食品、药品和化妆品法案》(FD&C法案)第201(s)节将“食品添加剂”定义为预期用途直接或间接产生或可能产生的任何物质,成为任何食品的成分或以其他方式影响任何食品的特性(包括用于生产、制造、包装、加工、制备、处理、包装、运输或保存食品的任何物质;以及用于任何此类用途的任何辐射源);如果该物质在1958年之前未被公认为安全(GRAS)或未经批准。[1]法规第409节将FCS定义为,如果该物质的用途不打算对此类食品产生任何技术影响,则其将用作制造、包装、运输或保存食品所用材料的成分。常见的食品接触物质包括涂料、塑料、纸张、粘合剂以及包装中发现的着色剂、抗菌剂和抗氧化剂。
FDA针对与
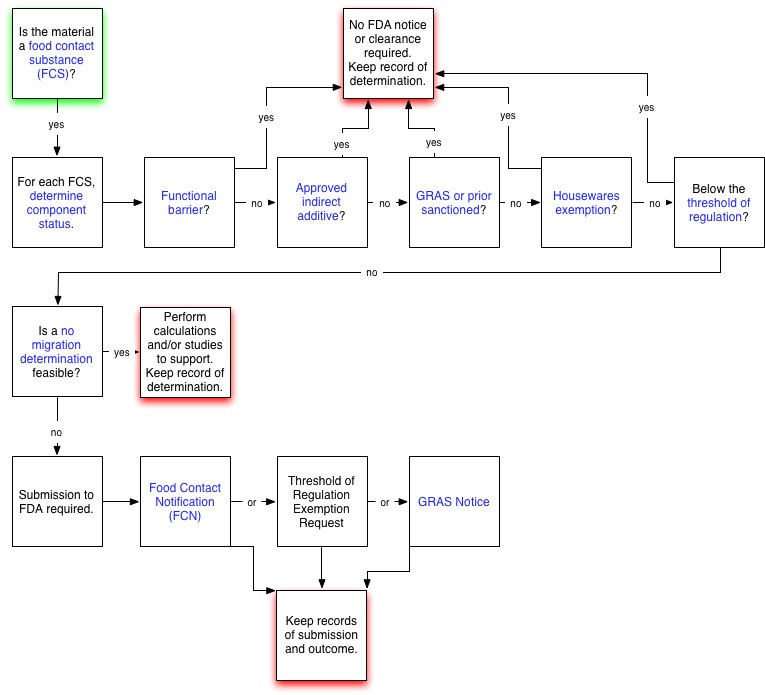
Inventory of Food Contact Substances Listed in 21 CFR
该数据库包含《美国联邦法规》(21 CFR)标题21中授权用于食品接触的物质清单。
该数据库包含关于物质特性的信息以及FDA针对特定预期用途和授权使用条件的规定。该清单包括食品接触物质(FCS),包括21 CFR第175-178、179.45和180.22部分中列出的间接食品添加剂,以及21 CFR 173中列出的二级直接添加剂,21 CFR 181中列出事先批准的食品成分,以及21 CF 186.1中公认为安全的物质
清单还包含21 CFR 189中列出的禁止用作食品接触物质的物质的信息。
除了《美国联邦法规汇编》第21卷授权和列出的成分外,美国食品和药物管理局还为根据《食品接触物质通知》(FCN)和《法规豁免阈值》(TOR)计划发布的食品接触物质的上市前授权保留了单独的库存。

FCN程序分为两种:
FCN许可具有一定的专属性,即只有FCN 的持有者才有权生产和销售该产品。一旦食品接触性企业取得FCN许可,则可增加企业竞争的砝码,取得固定的客户群,从而取得可观的经济效益。但是FCN申请的信息要求量大,专业性强,法规要求复杂,企业可以委托专业的咨询公司协助完成,从而可以缩短申请周期,提高申请成功率。
一个FCN可以涵盖多少种物质?
除了最初的FCN可以取代现有的请愿书,FDA通常只允许FCN覆盖一个FCS。如果公司有兴趣使用含有一种以上未清除物质的产品,则必须为每个未清除的FCS单独提交FCN。然而,并非FCS的所有组件都需要单独的FDA许可(例如,制造碱性树脂所需的物质,如催化剂);FDA根据具体情况解决了哪些部件需要放行的问题。
此外,可以为一类密切相关的聚合物获得单个FCN。
“配方FCN”单独处理(见下文),并假定配方所有组成部分的现有许可是管理局考虑的先决条件。

认证方式:
如果在收到完整的申请后,食品和药品管理局在120天内没有基于安全理由以书面形式反对该物质的使用,提交人及其客户可以合法地将该物质用于通知中规定的用途。FCN于第121天生效。
如果食品和药物管理局发现FCN提交文件“不完整”,将向通知人发送一封信,要求提供其认为对确定特定物质是否适合用于预期食品接触申请至关重要的数据。FDA通俗地将这些信件称为“缺陷信件”

FCN备案需要哪些类型的数据?
FCN必须包含足够的科学信息和数据,以证明FCS是安全的,FDA将其定义为“无害的合理确定性”,是FDA适用于所有食品添加剂的安全标准。在最初的食品接触材料请愿过程中也采用了同样的安全标准。FCN的要求与食品添加剂申请的要求基本相似。一般来说,通知应包括以下信息:
FCS及其杂质和FCS生产过程中残留反应物的化学特性,包括化学和结构式以及CAS注册号;
对物质制造过程的有力描述,包括用于确保过程一致性的制造规范;
FCS的预期使用条件;
在预期使用条件下可能成为食品成分的物质的数量和特性;
估计日常饮食中添加剂的浓度;
证明该摄入量安全性的毒理学数据;和
环境评估(在某些情况下)
提交人必须计算来自所有来源的潜在移民的累积估计膳食摄入量(CEDI),而不仅仅是相关产品,并为膳食中累积接触量超过0.5 ppb的物质提供支持性毒性研究。

